Soal No.1
Sebutkan faktor-faktor yang mempengaruhi kelarutan suatu zat? Jelaskan
PEMBAHASAN :
- Jenis pelarut, sifat polar dan non polar mempengaruhi kelarutan. Senyawa polar akan larut pada senyawa polar. Sedangkan senyawa non polar hanya akan larut pada senyawa non polar
- Suhu, saat suhu dinaikan, jarak antar molekul zat padat semakin renggang sehingga ikatannnya semakin lemah sehingga menjadi mudah larut dalam air. Sedangkan wujud gas naiknya suhu menjadi kurang larut karena gas akan mudah terlepas pada saat suhu dinaikan
Soal No.2
Tentukan rumus Ksp untuk senyawa berikut
- Ag2CrO4
- Cu2S
- PbI2
- Ca(OH)2
- CdS
LIHAT JUGA : Rangkuman Materi Ksp & Kelarutan
Soal No.3
Jika diketahui kelarutan gula adalah 1.800 gram/liter dan Mr gula = 360, tentukan kelarutan gula dalam satuan mol/liter
LIHAT JUGA : Video Pembelajaran Ksp & Kelarutan
Soal No.4
Jika hasil kali kelarutan AxBy = Ksp, tentukan kelarutan (s) dari AxBy
PEMBAHASAN :
Soal No.5
Diketahui kelarutan AxBy dalam air adalah s mol/liter. Tentukan Ksp AxBy
PEMBAHASAN :
AxBy ⇌ xAy+ + yBx-
s xs ys
Ksp = [Ay+]x[Bx-]y
Ksp = xsx. ysy
Ksp = xx.yy.s(x+y)
AxBy ⇌ xAy+ + yBx-
s xs ys
Ksp = [Ay+]x[Bx-]y
Ksp = xsx. ysy
Ksp = xx.yy.s(x+y)
Soal No.6
Jika pada suhu tertentu kelarutan PbI2 = 1 x 10-4 mol/L, tentukan Ksp PbI2
PEMBAHASAN :
PbI2 ⇌ Pb2+ + 2I–
s s 2s
Ksp = [Pb2+][I–]2
Ksp = s.(2s)2 = 4s3
Ksp = 4(1 x 10-4)3 = 4. 10-12
PbI2 ⇌ Pb2+ + 2I–
s s 2s
Ksp = [Pb2+][I–]2
Ksp = s.(2s)2 = 4s3
Ksp = 4(1 x 10-4)3 = 4. 10-12
Soal No.7
Jika Ksp Mg(OH)2 pada 25oC adalah 4 x 10-12, tentukan pH larutan jenuh Mg(OH)2
Soal No.8
Tentukan berapa gram PbI2 yang terdapat dalam 200 mL larutan jenuh PbI2 jika diketahui Ksp PbI2 = 1,6 x 10-8
Soal No.9
Diketahui kelarutan AgCl dalam air adalah 10-5 mol/L, tentukan berapa gram AgCl yang dapat larut dalam 250 mL air (Ar Ag =108; Cl = 35,5)
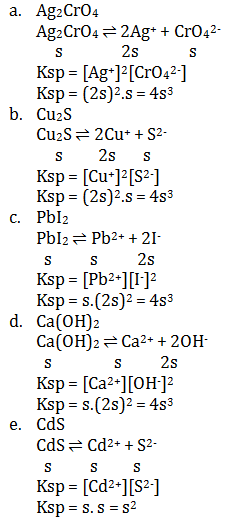

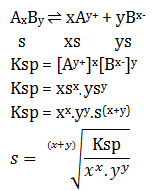
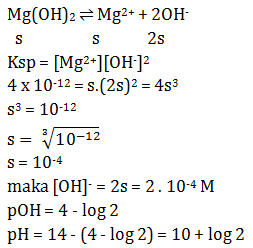
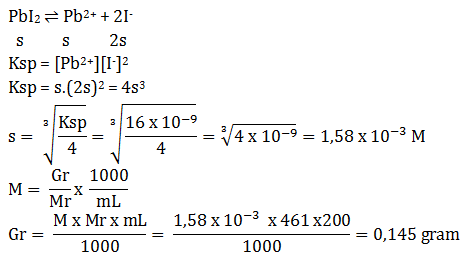
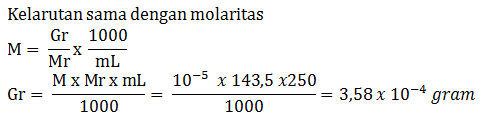
Tidak ada komentar:
Posting Komentar